03-5545-5400
溜池山王駅徒歩3分
赤坂駅徒歩5分
診察時間/9:00~12:00、13:30~17:00
休診/火曜、日曜、祝日 詳細はこちら

KYB CLINIC 幹細胞上清液
幹細胞上清液
幹細胞上清液治療について
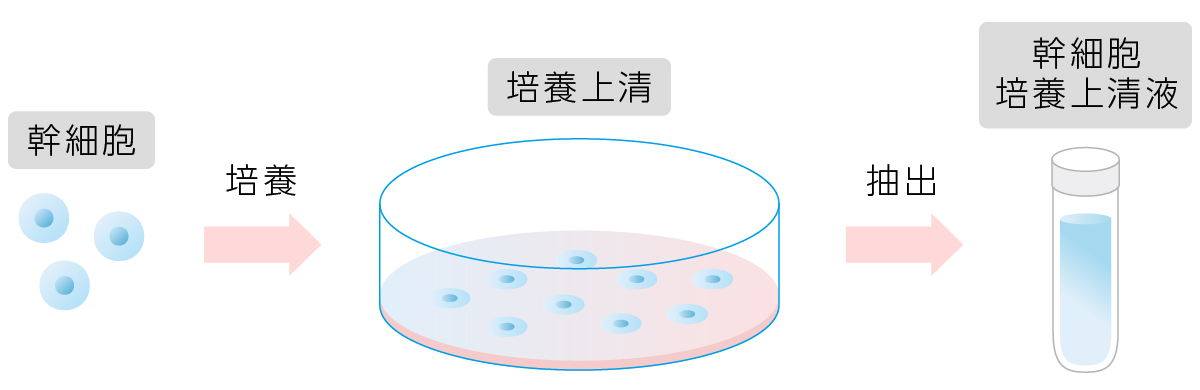
上清液は、幹細胞を培養した際に生じる上澄み液です。この液体には、エクソソームや成長因子などの有効成分が含まれており、抗炎症、再生促進、抗酸化、自己免疫力向上などの効果が期待されています。上清液は、点滴やスキンケア、化粧品、目薬などの形で応用され、未来の医療として注目されています。
再生医療の第一人者である上田実先生は、火傷治療中の培養皮膚研究において移植された表皮細胞が拒絶されても傷が同じ速度で治ることに注目しました。これにより、幹細胞が放出する信号分子が傷の治癒に関与していることが示唆されました。培養上清のみを用いた実験では、自家培養表皮と同様の治癒効果が観察され、培養上清中に存在する2,000種類以上のサイトカインなどのタンパク因子が幹細胞移植に匹敵する再生効果を持つことが確認されたのです。
幹細胞培養上清液は以前は不要物と考えられていました。しかし、この上清液には幹細胞から滲み出した有効成分が含まれているという仮説のもと、研究が進みました。今では、安全性を確保するために不純物を取り除き、ろ過や滅菌を行い、ウイルス検査に合格した製品が多くの医療現場で使用されています。
安全性について
当院で採用しているヒト幹細胞由来培養上清液は、医師問診によるドナー適格性が認められた20 ~ 30代の健康な日本人ドナーの組織から製造を行っており、ドナー選定や製造工程では数多くの安全性検査を実施しています。また出荷前判定は臨床培養士の有資格者がチェックをすることで安定性の高い製品提供を実現しています。
品質について
- 日本製品
へのこだわり - 安全性
へのこだわり - 臨床培養士
のチェック - 無調整
へのこだわり - 徹底した品質管理
安全検査
安全性を追求した3STEP検査を実施しています。
治療費用(税込)
- ※保険適用外(自費診療)となります。
- ※点滴手技料を含みます。
〒107-0052 東京都港区赤坂2-5-7 渡辺商事赤坂ビル6F
TEL:03-5545-5400
